FAQ Inwestora
Słuchamy waszych pytań, chętnie podejmujemy dialog i staramy się odpowiadać na wasze potrzeby. Właśnie dlatego przygotowaliśmy FAQ Inwestora SDS Optic S.A., czyli zestawienie najczęściej zadawanych przez was pytań (Frequently Asked Questions) wraz z wyczerpującymi odpowiedziami naszego Zarządu, kierownictwa oraz specjalistów z zespołów naukowych i administracyjnych.
Projekty realizowane przez SDS Optic S.A. należą do jednych z najbardziej zaawansowanych technologicznie. Skutecznie łączymy optoelektronikę (fotonikę) z biologią molekularną, immunochemią i inżynierią medyczną. Cieszymy się, że mimo skomplikowania technologii, procesów i kompetencji, tak żywo interesujecie się naszą Spółką oraz mikrosondą światłowodową inPROBE.
Jako Spółka publicznie notowana na rynku ASO NewConnect (prowadzonym przez Giełdę Papierów Wartościowych w Warszawie) zdecydowaliśmy się maksymalnie transparentną komunikację z naszymi akcjonariuszami oraz z osobami, które wspierają nas lub interesują się naszymi działaniami.
NAJCZĘŚCIEJ ZADAWANE PYTANIA
FAQ
Decyzję w tym zakresie pozostawiamy Państwu. Na pewno warto zainteresować się naszą działalnością. Mikrosonda światłowodowa do diagnostyki biomarkera HER2 dodatniego nowotworu piersi inPROBE jest innowacyjna i unikalna w skali globalnej. Tworzymy nowoczesną firmę, a nasz wyjątkowo interdyscyplinarny zespół naukowców i specjalistów codziennie udowadnia, że technologia inPROBE ma przyszłość.
Na firmowej stronie www i w kanałach social media prowadzimy transparentną komunikację, aby każdy zainteresowany mógł wyrobić sobie o nas własne zdanie.
Zachęcamy do obserwowania naszych profili z aktualnymi wydarzeniami:
1) Twitter: www.twitter.com/SDS_Optic (@SDS_Optic)
2) Linkedin: www.linkedin.com/company/sds-optic/ (@SDS Optic Inc.)
3) Facebook: www.facebook.com/sdsoptic/ (@sdsoptic)
4) Twitter inPROBE: https://twitter.com/OncoMicroprobe (@OncoMicroprobe)
6) Facebook inPROBE: https://www.facebook.com/inprobemedtech (@inprobemedtech)
7) YouTube SDS Optic: https://www.youtube.com/channel/UCHSL6UGD_AwaDKHJnXIM5lg
Pandemia, rosnąca inflacja oraz wydarzenia za naszą wschodnią granicą bezsprzecznie odciskają wyraźne piętno na sytuacji gospodarczej oraz kursach cen akcji spółek na całym świecie.
W Polsce sektor biotechnologiczny wciąż się rozwija. To specyficzny obszar, który ściśle łączy innowacyjne działy nauki z biznesem. Projekty Med-Tech oraz Bio-Tech wymagają cierpliwości, jednak w zamian, w dłuższym terminie mogą zaoferować atrakcyjne zyski. Z naszych obserwacji wynika, że polscy inwestorzy zdają sobie z tego sprawę i coraz chętniej inwestują w spółki biotechnologiczne.
Nie komentujemy kwestii kształtowania się kursu notowań akcji SDS Optic S.A. Niezależnie od bieżącej sytuacji na giełdzie, naszym głównym zadaniem jest realizacja założonej strategii i osiąganie kolejnych kamieni milowych, aby finalnie dostarczyć zwalidowany i bezpieczny produkt na rynek. Tym samym spełniamy obietnice złożone tym, którzy nam szczególnie zaufali – pacjentom, lekarzom i akcjonariuszom.
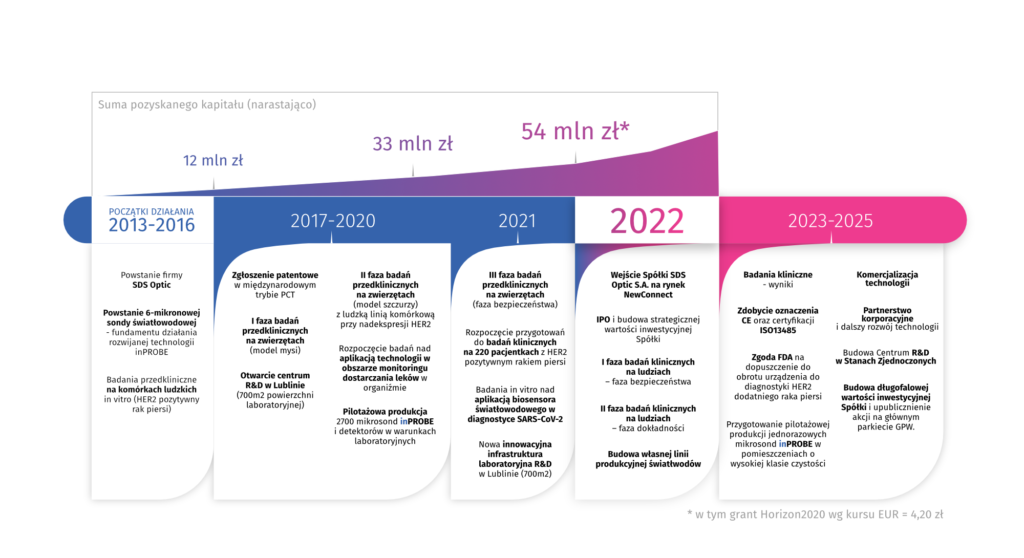
Do 2022 roku zainwestowaliśmy już niemal 54 mln PLN. Środki te stanowią zarówno wkład inwestorów prywatnych (w tym funduszy typu seed i venture capital), jak i dofinansowanie w ramach dotacji publicznych (w tym największa w historii polskich firm z sektora MŚP dotacja z Komisji Europejskiej w ramach programu SME Instrument Horizon 2020 w wysokości niemal 4 mln EUR).
Rozwój projektu jest możliwy także dzięki naszym akcjonariuszom. W czerwcu 2021 roku w ramach emisji akcji serii D, w pre-IPO pozyskaliśmy 11 mln PLN od inwestorów prywatnych, w tym renomowanych globalnych funduszy inwestycyjnych.
Więcej szczegółów na temat inwestycji SDS Optic S.A. znajdziesz w raportach okresowych: https://sdsoptic.pl/raporty-okresowe-spolki-sds-optic-s-a/
Nie wykluczamy kolejnych emisji, ponieważ to naturalny etap w rozwoju każdej spółki biotechnologicznej. Informowaliśmy o tym otwarcie już w trakcie naszych spotkań oraz prezentacji przy rundzie tzw. pre-IPO. Na ten moment zabezpieczyliśmy środki na kilkanaście miesięcy działania firmy. Mamy do dyspozycji także kolejne transze z dotacji unijnych, co daje pryzmat autonomii działania w długim okresie czasu oraz pewność osiągnięcia założonych kamieni milowych.
Nie zapadły żadne decyzje związane z konkretną datą kolejnej emisji. Teraz skupiamy się przede wszystkim na konsekwentnym realizowaniu zaplanowanych kamieni milowych i budowaniu wartości Spółki. W przypadku jakichkolwiek zmian w tym zakresie, będziemy komunikować je w raportach bieżących.
Aktualnie inPROBE to urządzenie rozwijane w obszarze detekcji biomarkera HER2 w dodatnim raku piersi. Projekt jest na etapie badań klinicznych, które potrwają do kilkunastu miesięcy. Jednocześnie wdrażamy także proces komercjalizacji inPROBE.
Zakończenie prac R&D mikrosondy inPROBE w bieżącym obszarze jej zastosowania (HER2+) planowane jest na przełomie lat 2023-2024, a składają się na to badania kliniczne oraz pełny proces certyfikacji ISO13485 oraz EU-MDR dla rynków Unii Europejskiej. Wartość pozostałej części zaplanowanej inwestycji wynosi ok. 5 mln PLN, a środki na ten cel mamy już zabezpieczone.
Rozwój projektów biotechnologicznych i zaawansowanych technologii medycznych łączy w sobie wiele składowych, wiele etapów oraz wiele ryzyk w zakresie wyników tych prac. Działania prowadzone przez nasz multidyscyplinarny zespół to jeden element. Do innych czynników, które wpływają na tempo działań, należą np. zewnętrzne instytucje, nadzorujące i regulujące proces badań klinicznych oraz docelowi użytkownicy naszego rozwiązania – lekarze i naukowcy.
Najważniejsze dla SDS Optic jest dostarczenie na rynek produktu bezpiecznego, skutecznego i zwalidowanego w badaniach klinicznych, a także dopasowanego do potrzeb użytkowników. Z tego powodu, na każdym etapie projektu rozpatrujemy wszystkie informacje zwrotne, które do nas trafiają i na bieżąco dostosowujemy nasze rozwiązania.
Przykładem takiej sytuacji są badania kliniczne, które w 2020 roku uniemożliwił wybuch pandemii koronawirusa – duże szpitale kliniczne zostały zamienione na szpitale jednoimienne, co wstrzymało całkowicie możliwość prowadzenia przez nas badań klinicznych.
Dodatkowo w maju 2021 r. weszło w życie zaktualizowane Rozporządzenie Parlamentu Europejskiego i Rady (UE) 2017/745 z dnia 5 kwietnia 2017 r. w sprawie wyrobów medycznych, zmiany dyrektywy 2001/83/WE, rozporządzenia (WE) nr 178/2002 i rozporządzenia (WE) nr 1223/2009 oraz uchylenia dyrektyw Rady 90/385/EWG i 93/42/EWG (MDR), do której dostosowaliśmy całą dokumentację kliniczną. Takie dostosowanie opóźnia rozpoczęcie badań ale w zamian daje gwarancję, że komercjalizowana technologia spełnia aktualne wymogi certyfikacji i walidacji, co znacznie zwiększy jej wartość w procesie komercjalizacji.
Po złagodzeniu obostrzeń, nasz zespół już na początku 2022 roku był gotowy do rozpoczęcia właściwych działań. W trakcie początkowych szkoleń przedklinicznych (styczeń-luty 2022) otrzymaliśmy od lekarzy wartościowe informacje zwrotne, związane z dodatkowym usprawnieniem procesu badania. Zdecydowaliśmy o wdrożeniu kilku usprawnień w manualnej części zabiegu, co zajęło kilka dodatkowych tygodni. Aby w pełni spełniać wszelkie wymogi regulacyjne podjęliśmy decyzję o złożeniu aktualizacji w odpowiednim urzędzie (URPL), z którym byliśmy w stałym kontakcie i od którego uzyskaliśmy końcowe zgody na wprowadzenie istotnych zmian w badaniu klinicznym pod koniec czerwca 2022 r. Finalnie największe znaczenie ma jakość produktu oraz jego bezpieczeństwo i funkcjonalność. Dodatkowo tym krokiem zwiększamy atrakcyjność technologii w środowisku medycznym, co przełoży się na jej wartość w procesie komercjalizacji.
Dzięki elastycznej formie rozwoju projektu, w której możemy łatwo reagować na zmiany, finalnie dostarczymy znacznie większą wartość, tak istotną dla końcowych użytkowników i naszych Akcjonariuszy.
Nasz model biznesowy opiera się na dwóch filarach:
• własna produkcja mikrosondy i sprzedaż urządzeń w ramach tworzonej własnej infrastruktury półprzemysłowej produkcji fotonicznych biosensorów;
• sprzedaż/licencjonowanie wydzielonej części technologii (wg obszaru zastosowania).
Już rozpoczęliśmy wdrażanie procesu komercjalizacji urządzenia inPROBE.
Aktualnie tworzona jest własna linia produkcyjna o mocy produkcyjnej do 50 tys. sztuk mikrosond rocznie. Zakończenie instalacji zamówionych przez Spółkę maszyn oraz uruchomienie zaawansowanych urządzeń produkcyjnych w dedykowanych do tego celu pomieszczeniach o kontrolowanych parametrach środowiskowych (tzw. Clean room) planowane jest do końca 2022 roku.
Na przełomie roku 2022/2023 rozpoczniemy zatem opracowanie zautomatyzowanych procesów produkcyjnych. Następnie przejdziemy do procesu certyfikacji i walidacji tych procesów, co na końcu ułatwi potencjalnym partnerom prowadzenie z nami rozmów w zakresie komercjalizacji oraz usprawni przyszłe skalowanie technologii.
Mikrosonda powinna trafić do sprzedaży zaraz po uzyskaniu certyfikacji (po wcześniej zakończonych badaniach klinicznych). Według aktualnie posiadanej przez nas wiedzy oraz szacunków naszego zespołu, przybliżony termin wprowadzenia produktu na rynek to przełom 2023/2024 roku. Termin ten może oczywiście ulec zmianie w przypadku wystąpienia nieprzewidzianych okoliczności.
Jednocześnie doprecyzowujemy techniczne kwestie związane z drugim filarem naszego modelu biznesowego, czyli pozyskanie partnera M&A, otwarcie placówki w USA oraz nawiązanie relacji z licencjonowanymi partnerami w zakresie produkcji i sprzedaży inPROBE za granicą.
Urządzenie medyczne inPROBE składa się z detektora oraz jednorazowej sondy w postaci biosensora światłowodowego. Aparatura służy do pomiaru in vivo (w organizmie pacjenta) poziomu stężenia konkretnej cząsteczki, markera lub bioaktywnego elementu, bez konieczności pobierania czy przygotowywania tkanki. Badanie trwa kilkadziesiąt minut, a zastosowane rozwiązania pozwalają badaczowi otrzymać obiektywne i dokładne, numeryczne wyniki w czasie rzeczywistym.

To rewolucja w skali światowej, porównywalna do wynalezienia rezonansu.
U podstaw zasady działania technologii leży opatentowana metoda hermetyzacji światłowodów, która pozwala połączyć rozwiązania fotoniczne z zaawansowaną biologią molekularną, inżynierią medyczną oraz immunochemią. Dzięki temu jesteśmy w stanie umieścić laboratorium histopatologiczne na czole światłowodu.
Rozwijana technologia inPROBE to przełom na rynku tradycyjnej diagnostyki in vitro (w laboratorium). Wyniki otrzymywane są znacznie szybciej (skrócenie czasu z tygodni do minut). Numeryczne dane są obiektywne i dokładne i nie ma tu miejsca na tzw. “błąd ludzki”. inPROBE może stanowić niezbędne uzupełnienie tradycyjnej biopsji, które pozwoli na dokładniejsze i szybsze postawienie diagnozy oraz wskazanie skutecznego leczenia.
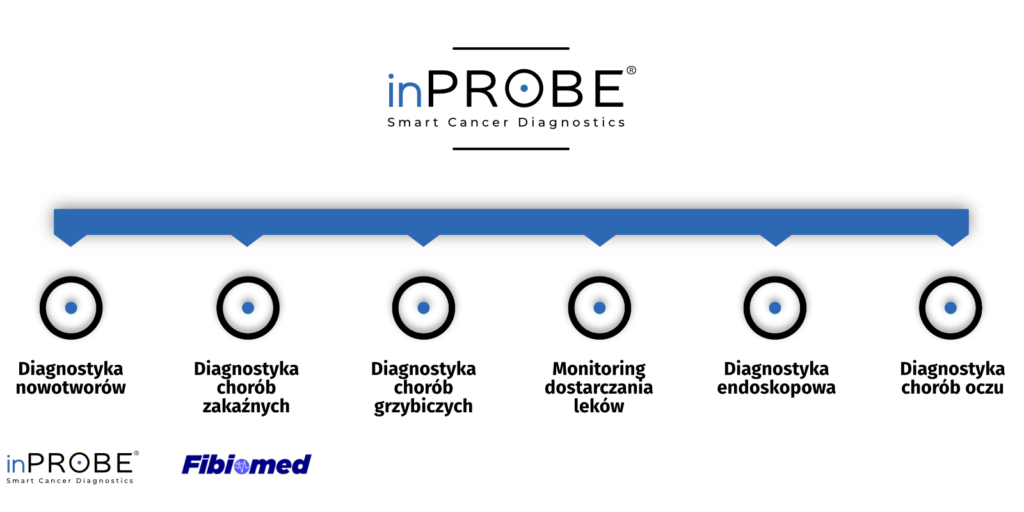
Obecnie zajmujemy się przede wszystkim aplikacją w obszarze diagnostyki HER2 w raku piersi. Nasze rozwiązanie wykazuje jednak znacznie większy potencjał, który zamierzamy wykorzystać.
inPROBE rozwijane jest jako skalowalna platforma technologiczna. W przyszłości może posłużyć do detekcji innych biomarkerów nowotworów (np. w nowotworach prostaty, żołądka, jelita grubego, płuc czy mózgu), chorób zakaźnych, takich jak koronawirus, a także chorób oczu (np. zwyrodnienie plamki żółtej, tzw. Wet-AMD) i chorób grzybiczych, w tym szczególnie groźnej sepsy, będącej wyzwaniem współczesnej medycyny.
Technologia inPROBE ma także ogromny potencjał zastosowania w procesie terapeutycznym, jako narzędzie do monitorowania skuteczności dostarczania leków w docelowe miejsce w organizmie. Z tym zastosowaniem wiąże się także kolejny obszar, jakim jest testowanie skuteczności nowych leków i ich wdrażanie na rynek. inPROBE w przyszłości może dostarczać niezbędnych informacji na temat dystrybucji leku w tkankach pacjenta. Dzięki temu gruntownie przebadane leki mogą być rozwijane i wdrażane na rynek znacznie sprawniej.
Jesteśmy na etapie doprecyzowania i wdrażania procesów produkcji oraz wewnętrznych procesów zarządzania. Do końca 2022 roku planujemy wdrożyć większość procesów i procedur pod kątem certyfikacji, także tych związanych z ISO (np. ISO13485). Na przełomie 2022 i 2023 roku planujemy rozpoczęcie testu i audytu pod kontrolą niezależnego, zewnętrznego podmiotu, który określi poziom wdrożenia niezbędnych norm i wymagań. Koniec audytu planowany jest na drugi kwartał 2023 roku.
Nasza światłowodowa mikrosonda inPROBE zgodnie z definicją Regulacji EU-MDR 2017/275 została zakwalifikowana jako wyrób medyczny stanowiący system, w którego skład wchodzi sterylna sonda oraz aktywne urządzenie medyczne z dedykowanym oprogramowaniem.
W maju 2021 roku weszła w życie nowa regulacja, tzw. EU-MDR. W związku z nowymi przepisami, przed badaniami klinicznymi, przeprowadzono wszystkie niezbędne testy i badania potwierdzające bezpieczeństwo użytkowania wyrobu zarówno dla personelu jak i pacjenta.
Po zakończeniu i podsumowaniu badań klinicznych, które obecnie jest planowane na 2023 rok, Spółka przystąpi do oceny zgodności z wymaganiami regulacji europejskiej EU-MDR 2017/275. Audyt zostanie przeprowadzony we współpracy z uprawnioną w tym zakresie Jednostką Notyfikowaną. Uzyskanie certyfikatu EU-MDR daje prawo do oznakowania inPROBE znakiem CE, zgłoszenia wyrobu, a następnie uzyskania pozwolenia z Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych w Warszawie na wprowadzenie wyrobu do obrotu.
Do uzyskania certyfikatu na zgodność z EU-MDR niezbędne jest potwierdzenie, że firma posiada wdrożony i dobrze funkcjonujący System Zapewnienia Jakości. SDS Optic S.A. jest na etapie wdrażania procedur zdefiniowanych w normie ISO EN 13485 dedykowanej dla producentów wyrobów medycznych. Spełnienie wymagań tej normy potwierdza, że producent jest zdolny do dostarczania wyrobów medycznych oraz usług z nimi związanych tak, aby spełniały wymagania prawne, gwarantowały deklarowaną jakość i powtarzalność procesu produkcji oraz spełniały oczekiwania klientów. Spółka zdefiniowała kluczowe oraz pomocnicze procesy w organizacji, dla których powstaje niezbędna dokumentacja systemowa.
Równolegle prowadzimy działania, mające na celu spełnienie regulacji Amerykańskiej Agencji ds. Żywności i Leków (FDA), w ramach procedury tzw. „Pre-Submission Meeting” oraz przy wsparciu naszych konsultantów ze Stanów Zjednoczonych.
SDS Optic S.A. przyjęło konkretną politykę publikacji naukowych, która nierozerwalnie wiąże się z prawami własności przemysłowej Spółki oraz polityką poufności danych.
Poniżej zamieszczamy listę wybranych publikacji oraz praw patentowych:
https://pubmed.ncbi.nlm.nih.gov/29775855/
https://pubmed.ncbi.nlm.nih.gov/33922995/
https://worldwide.espacenet.com/patent/search/family/053396751/publication/PL406533A1?q=PL406533A1
W planach Spółki są kolejne publikacje naukowe, połączone z harmonogramem wprowadzania technologii inPROBE na rynek, z jednoczesnym zachowaniem wdrożonej strategii zarządzania własnością intelektualną (tzw. IP Strategy), która m.in. zdefiniowała wybrane kluczowe elementy technologii, stanowiące wyłączny know-how Spółki, i które nie będą podlegały zastrzeżeniom w ramach zgłoszeń patentowych. W naszej ocenie takie podejście na pewno zwiększa atrakcyjność procesu komercjalizacji dla potencjalnych partnerów korporacyjnych.
inPROBE ma potencjał do zastosowania w wielu różnych obszarach, w tym do testowania efektywności nowych leków i terapii celowanych. Dzisiejsze techniki nie pozwalają w szybki sposób sprawdzić, czy kandydat na lek dociera do leczonego miejsca (np. okolic guza). inPROBE szybko i precyzyjnie wskaże, czy lek dociera w odpowiednie miejsce, a także w jakim stężeniu.
Naszą ambicją jest doprowadzenie do zaliczenia urządzenia medycznego inPROBE do listy FDA (w kat. companion diagnostics). Na liście tej znajdują się testy przypisane do konkretnych nowotworów i do terapii anty-nowotworowych, komercjalizowane przez konkretne firmy farmaceutyczne (najczęściej z grupy „Big Pharma”).
Dla sektora biotechnologicznego atrakcyjne może okazać się także zastosowanie technologii monitorujących pacjentów w trakcie całego procesu leczenia z jednoczesnym dostępem do danych o stężeniu zarówno docierającej aktywnej cząsteczki danego leku, jak i o stężeniu celowanego biomarkera nowotworowego – i to w czasie rzeczywistym, bez konieczności biopsji tkanki (której zgodnie z praktyką nie można dokonywać zbyt często).
inPROBE wykazuje potencjał zastosowania w mierzeniu stężenia zarówno cząsteczki aktywnej kandydata na lek, jak i cząsteczek aktywnych leków już dopuszczonych do obrotu.
Monitoring dostarczania leków to szeroki obszar badań oraz uwagi całego rynku tzw. Big Pharma. inPROBE wyróżnia się wśród dostępnych metod także tym, że nie wymaga stosowania żadnych znaczników, ani podawania dodatkowych związków, które często stosuje się podczas monitorowania transportu leków. Nie wymaga również stosowania drogich i skomplikowanych technologii obrazowania, np. rezonansu magnetycznego (MRI) czy tomografu (CT), które coraz częściej wykorzystywane są do monitorowania skuteczności prowadzonych terapii antynowotworowych.
SDS Optic S.A. na bieżąco monitoruje rynek, a także prowadzi regularny dialog z jednostkami medycznymi, naukowcami, lekarzami i pacjentami oraz przedstawicielami biznesu w sektorze biotechnologii i technologii medycznych. Tworzymy technologię w służbie człowieka, która odpowiada na konkretne potrzeby i oczekiwania odbiorców.
Najważniejsze korzyści inPROBE
Dla szpitali, klinik, laboratoriów i firmy:
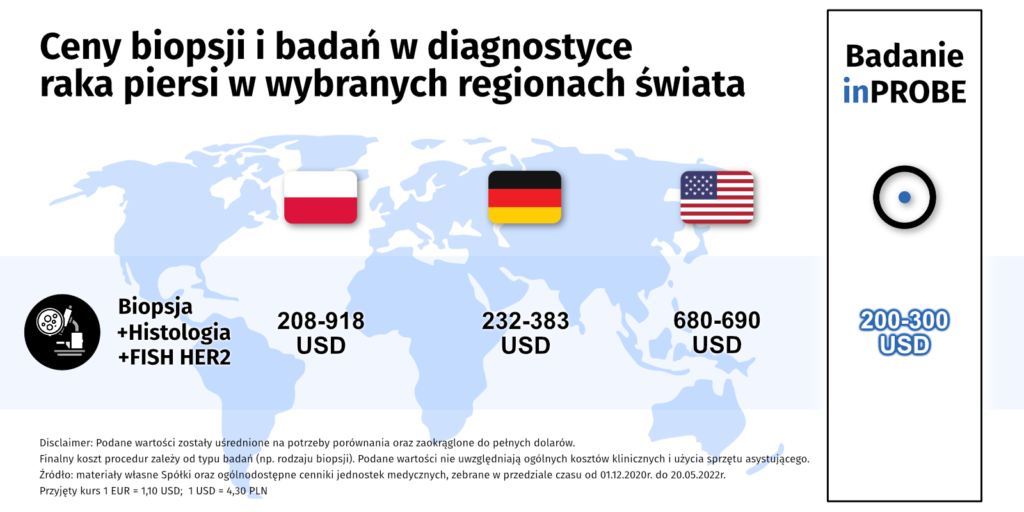
– Zmniejszenie kosztów diagnostycznych o min. 50% (z ok. €600 do ok. €300)
– Brak konieczności zakupu wielu drogich urządzeń (urządzenie detekcyjne inPROBE to jednorazowy koszt ok. €25 tys.)
– Uniknięcie konsekwencji prawnych w związku z fałszywymi wynikami diagnostycznymi (często miliony $/€ w odszkodowaniach)
Dla lekarzy:
– Dokładne i obiektywne wyniki numeryczne (diagnostyka nieoparta na obrazie)
– Redukcja fałszywie +/- wyników diagnostycznych
– Wyniki w czasie rzeczywistym (15-20 min)
– Metoda łatwa w użyciu, procedura manualnie zbliżona do znanej lekarzowi biopsji
Dla pacjentów:
– Mniej bolesne badanie (brak biopsji tkanki)
– Mniejszy stres w związku z natychmiastowym wynikiem i rekomendacją terapeutyczną
– Większy komfort życia w trakcie procesu terapeutycznego

4 lutego 2017 roku WHO z okazji Światowego Dnia Raka opublikowało nową listę rekomendowanych procedur i usług medycznych koniecznych do zastosowania na wczesnym etapie rozwoju choroby w celu zwiększenia szansy na wyleczenie pacjentów z nowotworem.
Głównym wnioskiem była konieczność globalnego silnego rozwoju wczesnej diagnostyki chorób nowotworowych, która ratuje życie oraz znacznie redukuje wydatki związane z leczeniem.
Aktem, który ma motywować rządy krajów na całym świecie do powyższych działań są tzw. cele zrównoważonego rozwoju (SDG – Sustainable Development Goals). Jednym z ich punktów jest ograniczenie przedwczesnych zgonów spowodowanych nowotworami o ⅓ do 2030 roku.
Zbliżony cel w 2021 roku wpisany został w misję Komisji Europejskiej związanej ze zwalczaniem chorób nowotworowych “Horizon Europe”: “goal of improving the lives of more than 3 million people by 2030, through prevention, cure and for those affected by cancer including their families, to live longer and better”.
SDS Optic S.A. mocno utożsamia się z tą misją, dlatego tworzymy i rozwijamy technologie do diagnostyki chorób nowotworowych, zakaźnych i grzybiczych. Wizja “zwiększenie przeżywalności na raka o 30% do 2030 roku” nierozerwalnie wpisało się w DNA naszej firmy. Łączy i motywuje cały nasz zespół.
Podstawa wizji firmy: zwiększenie przeżywalności na raka o 30% do 2030 roku
Źródło: https://www.who.int/news/item/03-02-2017-early-cancer-diagnosis-saves-lives-cuts-treatment-costs
Misja Komisji Europejskiej jest spójna z wizją spółki SDS Optic S.A.
Źródło:
https://ec.europa.eu/info/sites/default/files/research_and_innovation/funding/documents/cancer_implementation_plan_for_publication_final_v2.pdf
Biopsja (tj. pobranie tkanki) jeszcze bardzo długo będzie konieczna do określenia stanu zaawansowania choroby nowotworowej. inPROBE pozwoli na określenie poziomu badanego markera nowotworowego lub innej istotnej w diagnostyce substancji. Naszym celem nie jest zastąpienie biopsji, ale raczej jej uzupełnienie i dodanie do obecnej ścieżki diagnostycznej Pacjenta urządzenia, którego dotychczas brakowało lekarzom i naukowcom.
Po szybkiej diagnozie występowania i stężenia konkretnego markera możliwe będzie wdrożenie odpowiedniego leczenia celowanego. W sytuacji, gdzie czas gra kluczową rolę dla powrotu do zdrowia, to niezwykle istotne, aby lekarz mógł jak najszybciej skierować pacjenta na odpowiednią terapię celowaną.
Chcemy także wspierać laboratoria histopatologiczne, którym zależy na dodatkowej obiektywnej weryfikacji wyników diagnostycznych, oraz którzy poszukują nowych metod i technik w swojej pracy.
Mikrometryczna sonda światłowodowa inPROBE to jedyna w swoim rodzaju technologia na świecie, która łączy zaawansowaną fotonikę z biologią molekularną i inżynierią medyczną. Do tej pory na rynku nie istnieje żadne istotnie podobne komercyjne rozwiązanie, które pozwoliłoby w czasie rzeczywistym określić, czy i w jakim stężeniu w ciele pacjenta występuje dana cząsteczka (np. biomarker nowotworowy).





Badania, które pozwalają określić stężenie markera nowotworowego już istnieją, jednak dostępne badania pozwalają na diagnostykę z próbki krwi jedynie „krążących markerów nowotworowych” (CTCs) lub tzw. śladów genetycznych komórek nowotworowych (tumor ctDNA). Nie są to rozwiązania tak miarodajne, jak nasza technologia mierzenia stężenia cząsteczki w bliskiej okolicy guza.
Ciekłe/płynne biopsje (liquid biopsy) to kolejne pole zastosowania mikrosondy inPROBE. Na wczesnym etapie ciekłe biopsje stanowią dobre narzędzie do badań przesiewowych, czyli wstępnej identyfikacji pacjentów, u których podejrzewane jest wystąpienie choroby. Na jej podstawie nie jesteśmy jednak w stanie określić, gdzie jest zlokalizowany guz oraz jak się rozwija. Same badania ciekłej biopsji są obecnie również bardzo kosztowne (od kilku do kilkunastu tys. złotych) i w większości krajów nie są refundowane. Więcej zidentyfikowanych pacjentów można skierować na kolejny, bardziej zaawansowany etap diagnostyki, na którym to właśnie inPROBE pomoże odpowiedzieć na pytania, jakiego rodzaju nowotwór się rozwija oraz jakie leczenie jest niezbędne, aby uratować komuś zdrowie lub życie.
Główny parkiet zdecydowanie jest idealnym miejscem dla tak innowacyjnych przedsięwzięć, jak inPROBE. Wierzymy w naturalny rozwój Spółki, dlatego w pierwszej kolejności zdecydowaliśmy się wejść na rynek ASO NewConnect. Chcemy odpowiednio i stopniowo przygotować wszystkie struktury organizacyjne do sprawnego i koherentnego działania na giełdzie. Ten czas ma nam pomóc w wypracowaniu najlepszych praktyk w zakresie Corporate Governence czy wewnętrznych procesów organizacji. Będzie to miało fundamentalne znaczenie przy wejściu Spółki na główny rynek.
Rozważamy również tzw. dual-listing na jednej z giełd zagranicznych, aby zwiększyć zasięg i umożliwić dostęp do inwestycji w akcje SDS Optic S.A. inwestorom zagranicznym.
Dzisiaj skupiamy się na nowotworach piersi, ponieważ ich przypadków stwierdza się każdego roku najwięcej. W 2020 roku International Agency for Research on Cancer zidentyfikowało niemal 2,3 mln nowych przypadków nowotworów piersi. Jednocześnie, w tym samym roku rak piersi zabrał życie niemal 700 tys. pacjentów.
HER2 dodatni rak piersi to bardzo agresywna postać, którą diagnozuje się w ok. 20% przypadkach nowotworów piersi. To jednocześnie jeden z tych typów nowotworów, które przy wczesnej diagnozie dobrze reagują na terapie celowane (terapie dobrane do podtypu nowotworu), co często umożliwia pełne wyleczenie.
Wierzymy, że bezbłędna diagnostyka w czasie rzeczywistym pozwoli lekarzom szybciej reagować i podejmować właściwe decyzje związane z terapiami celowanymi. Sprawne rozpoczęcie odpowiedniego leczenia pozwala uratować zdrowie i życie znacznie większej liczby pacjentów na całym świecie.
Mówiąc jednym zdaniem: HER2 dlatego, że na ten typ nowotworu opracowano skuteczny celowany lek, którego wysoka skuteczność ściśle zależy od podania w odpowiednio szybkim czasie.
Dane na temat nowotworu piersi
Źródło: https://gco.iarc.fr/today/data/factsheets/cancers/20-Breast-fact-sheet.pdf
Źródło: https://www.breastcancer.org/pathology-report/her2-status
Faza I – bezpieczeństwa
Wszystkie procedury niezbędne do I fazy badań klinicznych inPROBE są gotowe. W badaniu bierze udział 18 pacjentek z nowotworem piersi. Po zaakceptowaniu zmian w zakresie manualnych działań lekarzy w trakcie zabiegu, pierwsza pacjentka pod narkozą zostaje poddana badaniu mikrosondą inPROBE. Na tym etapie potwierdzane jest bezpieczeństwo stosowania technologii u ludzi. Czas trwania tego etapu szacujemy na ok. 3-5 miesięcy, jednak zależy on w dużej mierze od lekarzy i terminów zabiegowych wyselekcjonowanych pacjentów.
Faza II – dokładności pomiaru
Po zakończeniu fazy I i dokładnej analizie uzyskanych wyników oraz obserwacji klinicznych rozpoczynamy fazę II. Weźmie w niej udział 196 pacjentek. Na tym etapie badana będzie dokładność pomiaru oraz niezbędne ustawienia kalibracyjne urządzenia. Podobnie jak w przypadku I fazy badań klinicznych, czas trwania etapu II zależy przede wszystkim od harmonogramu badań wybranych do programu pacjentów oraz od lekarzy prowadzących badania. Szacowany przez nas czas trwania tej fazy to ok. 6-8 miesięcy.
Nad procesem badań klinicznych czuwa profesjonalna firma CRO.
Zaczynamy naturalnie od Polski. To tutaj już oficjalnie certyfikowany wyrób medyczny inPROBE pojawi się w pierwszej kolejności. Polem pierwszej aplikacji będzie diagnostyka raka piersi pod kątem obecności markera HER2. Powołana została już także Spółka celowa FiBioMed, która pracuje nad technologią do diagnostyki chorób zakaźnych, w tym koronawirusa. Prowadzimy także rozmowy z przedstawicielami tzw. BigPharma w temacie potencjalnego przyszłego wykorzystania inPROBE do monitorowania transportu leków w organizmie (drug delivery monitoring), co będzie miało także wielką wartość w kontroli terapii celowanych, stosowanych przy leczeniu nowotworów.
Kolejnymi rynkami, na które chcemy wprowadzić urządzenie inPROBE to zachodnie kraje Unii Europejskiej, Stany Zjednoczone oraz kraje azjatyckie. Pracujemy nad tym, aby nasze urządzenie spełniało w pierwszej kolejności wszystkie wymagania przepisów polskich, unijnych oraz docelowo regulacje amerykańskiej organizacji FDA.
FiBioMed, spółka celowa powołana do życia z inicjatywy Założycieli SDS Optic S.A. i pomysłodawców rozwiązania inPROBE, zajmuje się opracowaniem rozwiązania, które docelowo pozwoli w jednym czasie zdiagnozować wiele różnych chorób zakaźnych (nie tylko aktualnie groźnego koronawirusa), a więc potrzeba jej wykorzystania będzie zawsze. Wśród nas występuje wiele różnych wirusów przez cały rok, a nie tylko sezonowo.
Nawet jeśli świat zażegna stan epidemii i pandemii Covid-19, koronawirus najprawdopodobniej pozostanie z nami na dłużej. To w dalszym ciągu będzie wymagało szybkiej i dokładnej diagnostyki, która pozwoli podjąć odpowiednie kroki w celu zastosowania odpowiedniej ścieżki leczenia. Dodatkowym impulsem będzie dostęp do technologii pozwalającej na diagnozowanie prawie 100 próbek w jednym czasie co będzie wspierać duże miasta i duże ośrodki w zarządzania pandemią oraz w podejmowaniu decyzji o tzw. lock-downach.
Tworzymy technologię, która będzie dostępna w momencie wybuchu kolejnej pandemii. Technologię, która będzie mogła być szybko przeskalowana i skomercjalizowana, tak jak to miało miejsce ze szczepionkami opartymi o technologię mRNA (opracowywane przez wiele lat, użyte w walce z pandemią w kilka miesięcy przy wsparciu globalnego partnera korporacyjnego).
inPROBE to platforma technologiczna. To oznacza, że pracujemy nad rozwiązaniem, które będzie można szybko i efektywnie przeskalować na inne zastosowania, inne choroby zakaźne. Biologia niesie znaczne ryzyko, że w przyszłości pojawią się kolejne epidemie i pandemie, a także nowe wirusy, do których diagnostyki w dużym stopniu już będziemy przygotowani. W razie potrzeby, będziemy w stanie sprawnie przetransponować inPROBE na odpowiedni obszar aplikacji.
Gdzie znajdę więcej informacji o Spółce SDS Optic S.A.?
Nasza firma dąży do zachowania pełnej transparentności swoich działań, w poszanowaniu naszych odbiorców oraz wymogów związanych z naszą obecnością na rynku NewConnect. Więcej informacji o SDS Optic S.A. można znaleźć przede wszystkim na naszej stronie: www.sdsoptic.pl
Relacje inwestorskie
Komunikacja z naszymi akcjonariuszami, inwestorami oraz osobami zainteresowanymi naszą obecnością na giełdzie (w tym niezbędne informacje oraz zapis na specjalny Newsletter Inwestorski) są dostępne na stronie https://ir.sdsoptic.com
Mikrosonda światłowodowa inPROBE
Jeśli chcesz dowiedzieć się więcej o rozwijanej w SDS Optic S.A. technologii, zobacz dedykowaną stronę poświęconą światłowodowej mikrosondzie do diagnostyki in vivo w obszarze HER2 dodatnich nowotworów piersi, w czasie rzeczywistym: www.inprobe.com




